對於(yu) 已經進入 A2階段的考生而言,輾轉於(yu) 學術端與(yu) 升導端之間是學習(xi) 生活的常態,對應的學術任務和升學細節都需要相當程度的把握和規劃。與(yu) AS階段更偏向於(yu) 穩固根基的學科知識不同,A2階段的學習(xi) 往往更加注重綜合性,而且是進一步向更深層次的大學課程靠攏的。
以化學 U5為(wei) 例,其涉及的考點數量與(yu) 內(nei) 容的抽象程度是銜接大學課程的典型代表。本篇將由 G5教研部 Ezra老師結合更新考綱要點以及內(nei) 部整合的考點講義(yi) ,為(wei) 大家梳理化學 U5中的各大重難點。
考點分布
題型架構
『氧化還原平衡專(zhuan) 題』
首先是第一模塊的氧化還原平衡專(zhuan) 題,其中涉及的電化學知識是部分新接觸化學U5的考生會(hui) 感覺相對抽象的內(nei) 容。實際上,根據氧化還原的知識點進行推導,結合化學U4中thermodynamic feasibility熱力學可行性的概念並不難把握考點的核心。在明確了standard hydrogen electrode標準氫電極對於(yu) standard electrode potential標準電極電勢的參照方式後(電池作圖還需注意規範),其電極判定核心原則可記為(wei) :電子由anode流出,發生oxidation,即發生氧化反應的電極為(wei) anode。易混淆的概念為(wei) ,anode在原電池中被稱為(wei) negative electrode/terminal負極,在電解池中被稱為(wei) positive electrode陽極,相同點為(wei) 兩(liang) 者都是釋放電子的電極。
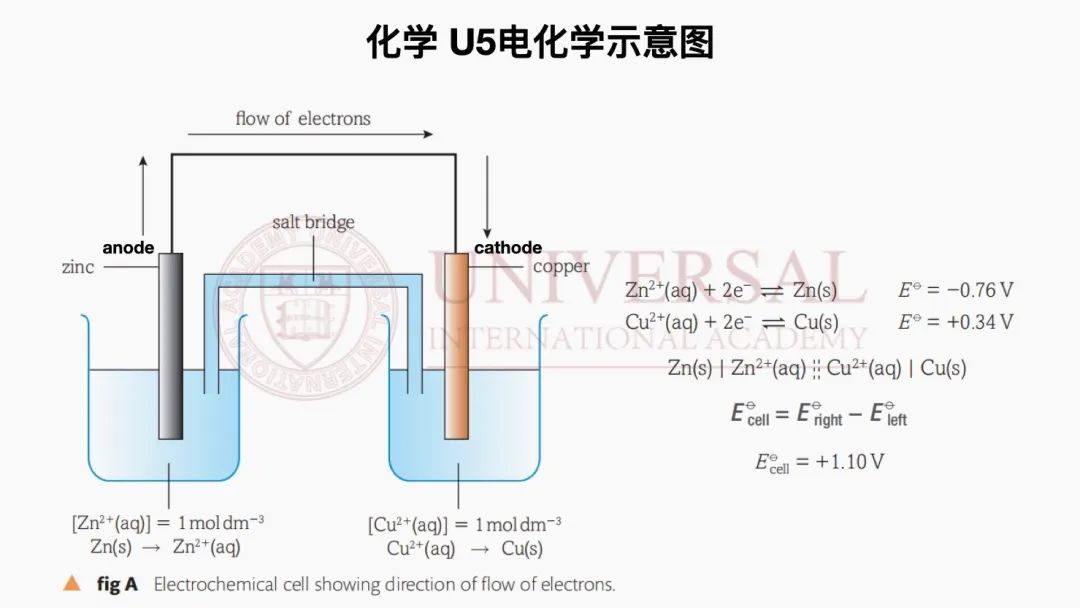 G5教研部化學 U5電化學專(zhuan) 題講義(yi) 截圖
G5教研部化學 U5電化學專(zhuan) 題講義(yi) 截圖
因此在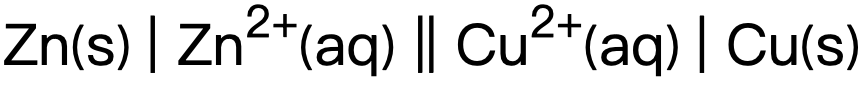 的電池中,
的電池中,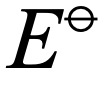 為(wei) 負值的half-cell
為(wei) 負值的half-cell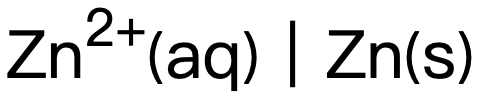 在原電池的左側(ce) ,half equation傾(qing) 向於(yu) 逆向移動,釋放電子,為(wei) anode。完整電池對應的electromotiveforce電動勢則應以電池書(shu) 寫(xie) 中的右側(ce) 半電池電勢 (此處為(wei)
在原電池的左側(ce) ,half equation傾(qing) 向於(yu) 逆向移動,釋放電子,為(wei) anode。完整電池對應的electromotiveforce電動勢則應以電池書(shu) 寫(xie) 中的右側(ce) 半電池電勢 (此處為(wei) 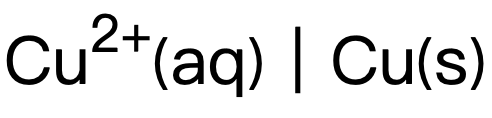 )減去左側(ce) 半電池電勢 (此處為(wei)
)減去左側(ce) 半電池電勢 (此處為(wei) 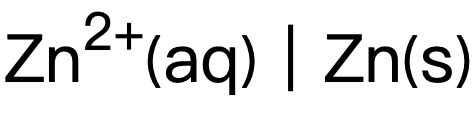 ),若最終得出的數值為(wei) 正,由於(yu)
),若最終得出的數值為(wei) 正,由於(yu) 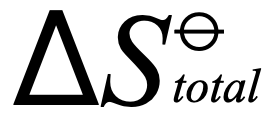 總熵與(yu)
總熵與(yu) 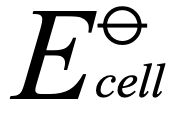 電動勢成正比,那麽(me) 該電池屬於(yu) thermodynamically feasible/unstable/spontaneous熱力學可行,而若電動勢為(wei) 負,則說明該電池屬於(yu) thermodynamically stable熱動力學不可行。G5教研部溫馨提示:真正獲得一個(ge) 正常運作的電池,還需low activation energy低活化能以確保kinetically unstable動力學可行。
電動勢成正比,那麽(me) 該電池屬於(yu) thermodynamically feasible/unstable/spontaneous熱力學可行,而若電動勢為(wei) 負,則說明該電池屬於(yu) thermodynamically stable熱動力學不可行。G5教研部溫馨提示:真正獲得一個(ge) 正常運作的電池,還需low activation energy低活化能以確保kinetically unstable動力學可行。
『過渡金屬相關(guan) 』
第二模塊涉及過渡金屬,即離子狀態下擁有未填滿3d orbitals的金屬元素,因此Zn和Sc並不屬於(yu) 過渡金屬,注意此處定義(yi) 中軌道為(wei) 複數 (即 s不可省略)。對於(yu) 過渡金屬溶液顯色的原因解釋屬於(yu) 高頻考點,需明確ligands配體(ti) 將3d orbitals分成兩(liang) 個(ge) energy levels,低能量層級的electron吸收對應光譜中的能量promote躍遷至高能量層級,對應的互補色complementary color得以顯現。
對於(yu) ligand配體(ti) 與(yu) 過渡金屬形成的complexes配合物 (包含 complex ion配離子),對應的命名應為(wei) “數量+配體(ti) 名+過渡金屬名+羅馬數字”,例: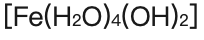 名稱為(wei) tetraaquadihydroxoiron(II)。一般情況下,由monodentate ligands單配位與(yu) bidentate ligands雙配位或multidentate ligands發生ligand exchange配體(ti) 交換反應,也就是物質 species個(ge) 數增多的情況是
名稱為(wei) tetraaquadihydroxoiron(II)。一般情況下,由monodentate ligands單配位與(yu) bidentate ligands雙配位或multidentate ligands發生ligand exchange配體(ti) 交換反應,也就是物質 species個(ge) 數增多的情況是 變大的體(ti) 現,生成物的穩定性也會(hui) 趨於(yu) 增強。
變大的體(ti) 現,生成物的穩定性也會(hui) 趨於(yu) 增強。

G5教研部化學 U5配離子專(zhuan) 題講義(yi) 截圖
集訓過程中最容易出現錯誤的考點之一莫過於(yu) 過渡金屬的各類反應式和實驗現象對應。簡單歸納,加入少量的 氨水或alkali堿,反應類型均為(wei) deprotonation去質子化 (即失去
氨水或alkali堿,反應類型均為(wei) deprotonation去質子化 (即失去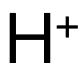 ),且失去的個(ge) 數與(yu) 過渡金屬價(jia) 位一致,對應生成沉澱。而此時upon standing靜置後被氧化會(hui) 有現象變化的包括
),且失去的個(ge) 數與(yu) 過渡金屬價(jia) 位一致,對應生成沉澱。而此時upon standing靜置後被氧化會(hui) 有現象變化的包括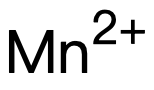 【由pale brown precipitate
【由pale brown precipitate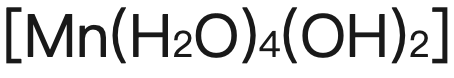 逐漸加深為(wei)
逐漸加深為(wei) 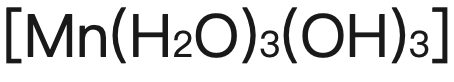 ,最終變成darkerbrown precipitate
,最終變成darkerbrown precipitate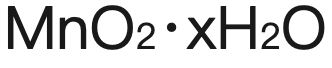 】;
】;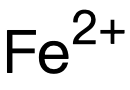 【由green precipitate
【由green precipitate
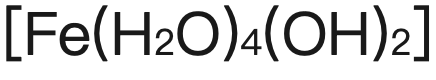 逐漸變成brown precipitate
逐漸變成brown precipitate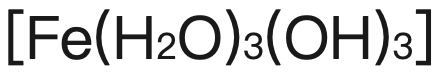 】;
】;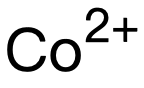 【由blueprecipitate
【由blueprecipitate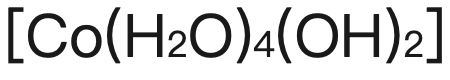 逐漸變成pink precipitate】。以上三種沉澱中隻有
逐漸變成pink precipitate】。以上三種沉澱中隻有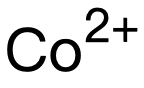 在繼續加入過量
在繼續加入過量 氨水後會(hui) 產(chan) 生pale yellow solution
氨水後會(hui) 產(chan) 生pale yellow solution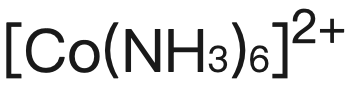 ,然後經氧化形成brown solution
,然後經氧化形成brown solution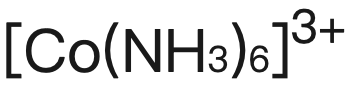 。涉及背記內(nei) 容較多,課後還需額外付出時間加深印象。
。涉及背記內(nei) 容較多,課後還需額外付出時間加深印象。
『有機化學:芳香烴』
關(guan) 於(yu) 芳香烴專(zhuan) 題最重要的就是苯環結構的對比,五個(ge) 方向整理如下,需認準六個(ge) 碳碳鍵擁有處於(yu) 單鍵與(yu) 雙鍵之間性質的原則,電子排布均勻同樣也是苯環相對穩定的原因之一。
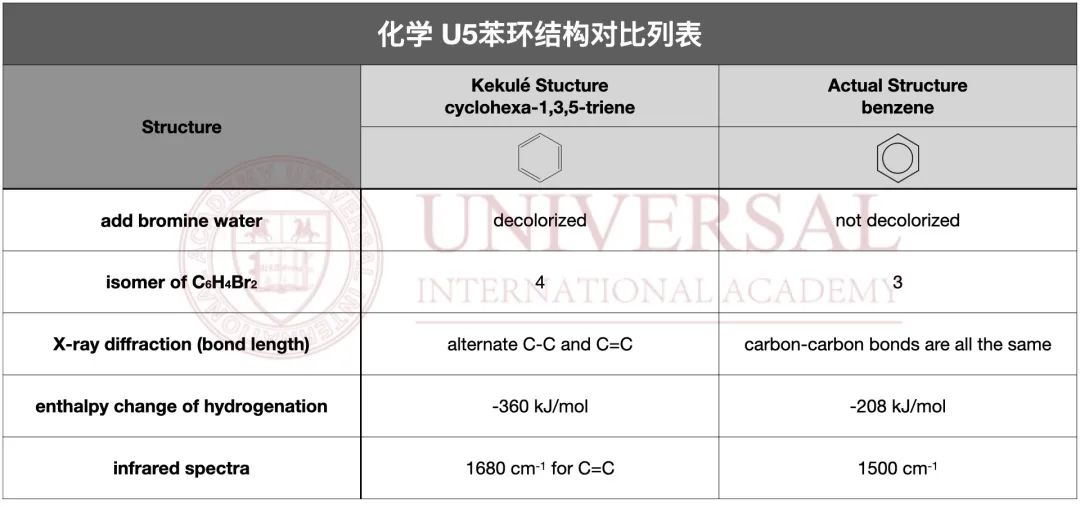
G5教研部化學 U5苯環專(zhuan) 題講義(yi) 截圖
而化學 U5中的機理其實隻有一種,無論是 bromination溴化、nitration硝化、alkylation烷基化還是acylation酰化,書(shu) 寫(xie) 邏輯一致,謹記箭頭方向為(wei) 電子走向。由於(yu) 苯環中的兩(liang) 個(ge) 電子被electrophile親(qin) 電體(ti) 所吸引,剩餘(yu) 2/3的圓弧和正電荷不可遺漏,且開口方向需與(yu) 添加基團方向一致,包括反應前後催化劑的消耗與(yu) 再生。
對比而言,phenol苯酚中氧原子提供的lone pair與(yu) 苯環形成更大的electron cloud,electron density電子密度增大,因此對於(yu) electrophile的吸引力也就更強,活性自然上升。苯環與(yu) 溴單質需要catalyst催化劑和heat under reflux加熱回流的條件,而苯酚則可在室溫下無需催化即可發生,產(chan) 生white precipitate白色沉澱 2,4,6-tribromophenol,溴水同樣褪色。
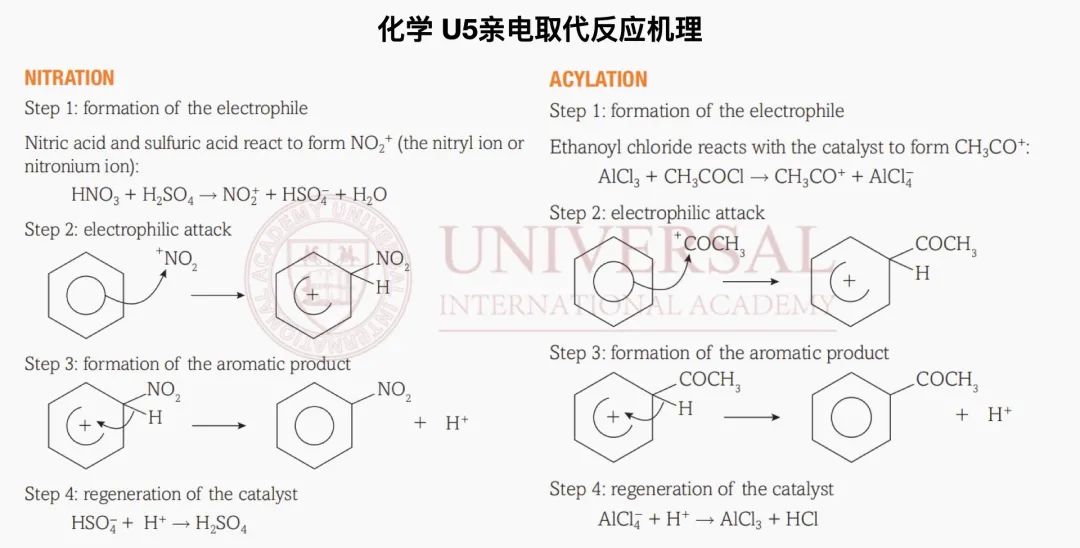
G5教研部化學 U5親(qin) 電加成專(zhuan) 題講義(yi) 截圖
『有機氮化合物』
第四模塊中對於(yu) 有機氮化合物的反應中 amine胺類的反應其實都可看作是 中的H被替換成對應的alkyl group烷基或benzene苯環,換句話說,反應邏輯與(yu)
中的H被替換成對應的alkyl group烷基或benzene苯環,換句話說,反應邏輯與(yu)  一致,思路不清時可進行對比參照。製取amine的方式分為(wei) aliphatic脂族和aromatic芳香族,前者對應從(cong) nitrile腈在lithium tetrahydridoaluminate四氫鋁鋰的dry ether幹醚 (幹燥環境避免將水還原為(wei)
一致,思路不清時可進行對比參照。製取amine的方式分為(wei) aliphatic脂族和aromatic芳香族,前者對應從(cong) nitrile腈在lithium tetrahydridoaluminate四氫鋁鋰的dry ether幹醚 (幹燥環境避免將水還原為(wei) 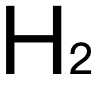 )環境下發生還原反應得到,後者則是由nitrobenzene硝基苯在Tin錫和concentrated hydrochloric acid濃鹽酸的還原作用下(還原劑為(wei) Tin和反應中生成的
)環境下發生還原反應得到,後者則是由nitrobenzene硝基苯在Tin錫和concentrated hydrochloric acid濃鹽酸的還原作用下(還原劑為(wei) Tin和反應中生成的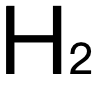 ),通過 heat under reflux最終得到。
),通過 heat under reflux最終得到。
而 azo dye重氮染料由於(yu) 其綜合性較強,同樣屬於(yu) 真題中會(hui) 高頻出現的考點。首先是極易分解的nitrous acid亞(ya) 硝酸需在低溫冰水溶液中將亞(ya) 硝酸鈉與(yu) 鹽酸混合當場製備,緊接著加入phenylamine在5°C以下的溫度中生成benzenediazonium ion重氮苯離子,否則將生成phenol。而benzenediazonium ion與(yu) phenoxide ion在堿性環境中反應,生成物在經過dilute hydrochloric acid酸化後將生成擁有conjugated system共軛係統(單雙鍵交替)的4-hydroxyphenylazobenzene,即azo dye重氮染料的一種,具有相當的穩定性,故其染色效果極佳。
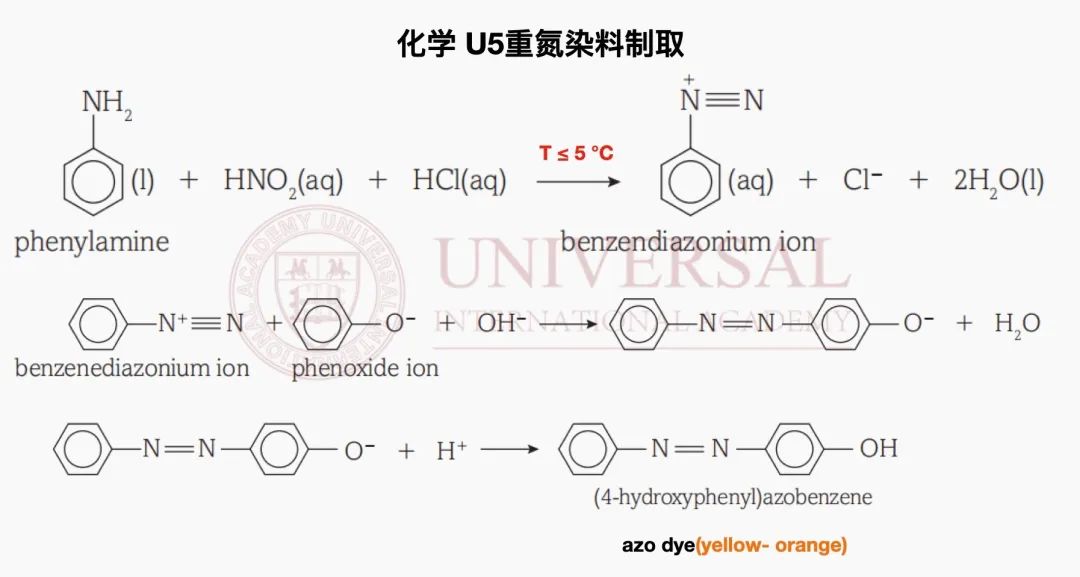
G5教研部化學 U5重氮染料專(zhuan) 題講義(yi) 截圖
氨基酸的 zwitterion兼性離子對應同時帶有正負電荷,但整體(ti) 不帶電的離子狀態。此時對應溶液的pH值被稱為(wei) isoelectric point等電點。酸性環境中,氨基酸將由amino group氨基體(ti) 現堿性,即得到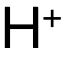 ;堿性環境中,氨基酸將由carboxylic acid羧酸體(ti) 現酸性,即失去/提供
;堿性環境中,氨基酸將由carboxylic acid羧酸體(ti) 現酸性,即失去/提供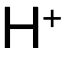 。另外在paper chromatography紙層析法中將developing agent顯影劑ninhydrin茚三酮記住即可,具有讓氨基酸顯色的功能。
。另外在paper chromatography紙層析法中將developing agent顯影劑ninhydrin茚三酮記住即可,具有讓氨基酸顯色的功能。
『有機合成』
最後一個(ge) 模塊為(wei) 有機合成,整體(ti) 來看其實是有機相關(guan) 內(nei) 容的總結,包括 alkene、halogenoalkane、alcohol、aldehyde、ketone、carboxylic acid和 phenol等物質的檢驗和結構分析,涉及化學U2中的mass spectra質譜圖和infrared spectra紅外光譜,以及化學U4中的NMR spectra核磁共振譜(包含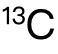 和proton)等內(nei) 容,並不屬於(yu) 新知識點,不過考慮到綜合性,連帶化學U1中empirical formula最簡式的運算和實驗操作中的hazard危害和risk風險都將是複習(xi) 集訓中不可輕視的考點。
和proton)等內(nei) 容,並不屬於(yu) 新知識點,不過考慮到綜合性,連帶化學U1中empirical formula最簡式的運算和實驗操作中的hazard危害和risk風險都將是複習(xi) 集訓中不可輕視的考點。
而有機合成中最為(wei) 值得重視的基礎考點之一就是碳鏈的延伸,目前共包含四種方式,第一種是 halogenoalkane鹵代烷與(yu) cyanide ion氰離子 (多由 KCN提供)在heat under reflux和 ethanol的條件下生成nitrile腈,較原來多出一個(ge) 碳。第二種則是將hydrogen cyanide氰化氫在堿性環境中加成到carbonyl compound羰基化合物上,同樣多出一個(ge) 碳。第三種則是將benzene通過催化劑的作用下與(yu) halogenoalkane發生alkylation烷基化反應,增加對應烷基中的碳原子個(ge) 數。
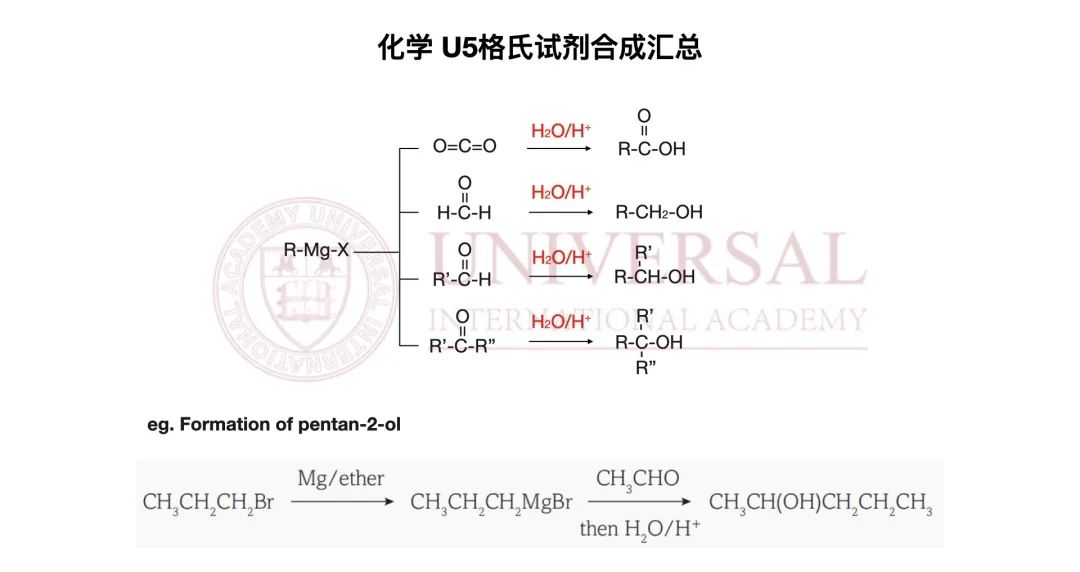
G5教研部化學 U5格氏試劑專(zhuan) 題講義(yi) 截圖
而第四種也就是本章的重點內(nei) 容,Grignard reagents格氏試劑,即通過 halogenoalkane鹵代烷 (一般為(wei) 溴代烷)、Mg鎂和dry ether幹醚在heat under reflux作用下得出的R-Mg-X。Grignard reagents分別能夠將 和carbonyl compound在酸性條件下最終轉化成對應的carboxylic acid和alcohol,同時增加bromoalkane中的碳原子個(ge) 數。
和carbonyl compound在酸性條件下最終轉化成對應的carboxylic acid和alcohol,同時增加bromoalkane中的碳原子個(ge) 數。
以上就是 G5教研部針對化學U5各個(ge) 章節中重難點的整合梳理,還需結合課堂摘錄和專(zhuan) 題練習(xi) 注意複習(xi) 回顧,考點網絡涉及較廣,清晰邏輯把握原理最為(wei) 關(guan) 鍵,預祝各位考生能夠在即將到來的五月留學統考中發揮出自己的最佳水平,向理想夢校更進一步!














評論已經被關(guan) 閉。